
日前,智能医学讲堂—智能医用材料青年学者沙龙在山东第一医科大学医学人工智能与大数据学院圆满举行。
山东第一医科大学放射学院赵鹏博士,受邀作了题为《 铁基纳米材料及其应用》的专题报告,分享他在铁基纳米材料领域的研究工作进展和成果。
铁基纳米材料的特点
铁基纳米材料是一种重要的过渡金属氧化物的功能性纳米材料,具有合成简单,修饰容易,功能化简便,形貌可控等优势。铁基纳米材料独特的理化性质及良好的生物相容性使其成为生物医学领域中应用最广泛的纳米材料之一,如应用在细胞分选、磁分离免疫检测、MRI造影、磁热疗、药物递送载体、多模态诊断等领域。随着研究的深入,铁基纳米材料越来越多的新的功能和应用潜力被开发出来。比如通过工程设计使纳米颗粒具有一种或多种酶的活性,模拟酶有远超生物酶的体内应用场景。又如铁基纳米材料可以促进间充质干细胞的成骨分化。
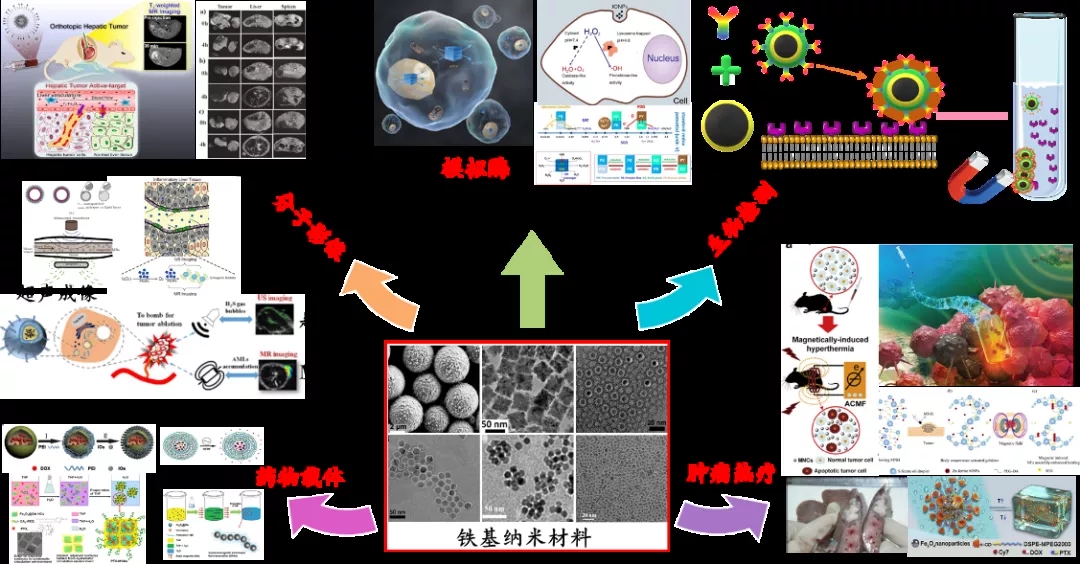
单核巨噬细胞的清除作用是铁基纳米材料体内应用的主要障碍
铁基纳米材料的生物医学应用可大致分为治疗和诊断,其中大部分为体内应用。遍布体内的单核巨噬细胞,会快速清除这些“异物”,致使铁基纳米材料在体内肝、脾等器官富集,造成其在体内应用的循环时间短、靶向有效性差,提高使用剂量又会造成安全性风险。单核巨噬细胞的清除作用严重制约纳米材料的体内应用。因此, 铁基材料在进行体内应用时,抗巨噬细胞内吞是进行材料设计的首要考虑因素。常规的方法是通过调控尺寸、形貌、表面电荷、表面化学修饰等性质来影响细胞对纳米颗粒的内吞。其中表面修饰是最重要的手段,常见的有是在纳米材料外修饰聚乙二醇(PEG),改变材料的亲疏水性,增加空间位阻来减少细胞的内吞。通过理化性质的手段只能非特异的减少所有细胞的内吞,那么 能否通过一种生物学的手段来选择性的减少巨噬细胞的内吞,这也是目前正在进行的工作。
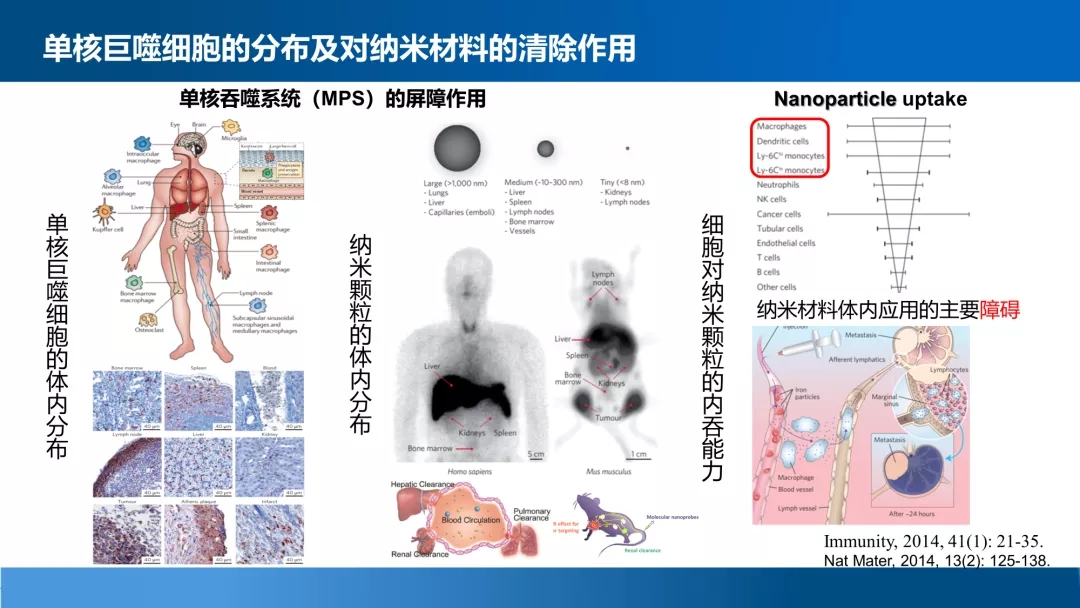
选择性抗巨噬细胞内吞的铁基纳米材料设计
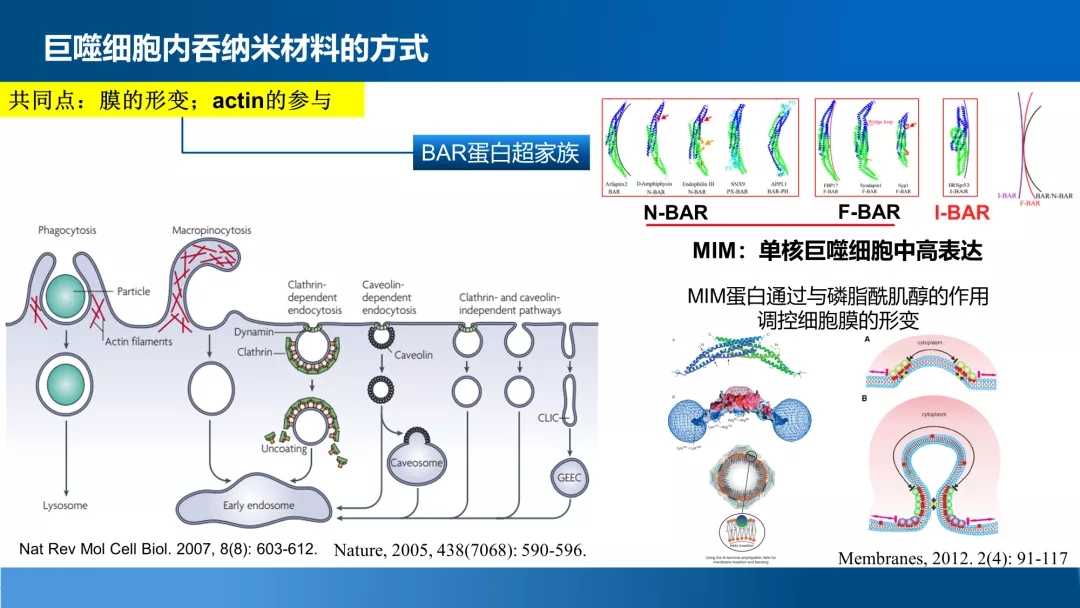
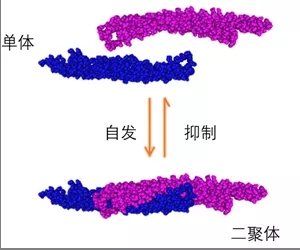
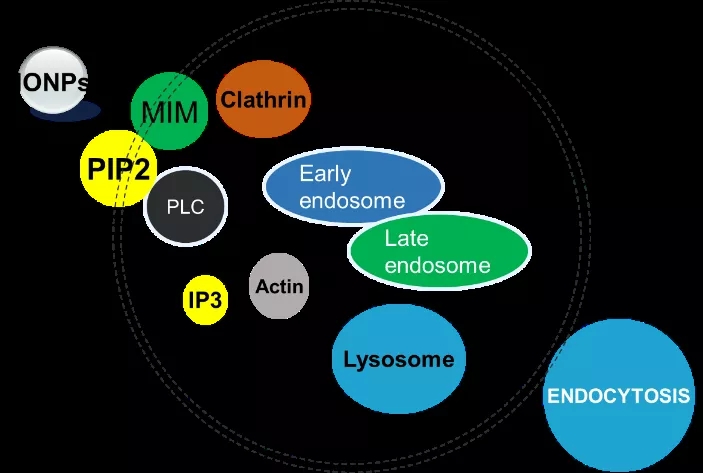
研究中,赵鹏课题组筛选出一种在单核巨噬细胞中特异高表达的内吞相关蛋白——MIM蛋白,而MIM蛋白在成体大多数组织与细胞中的表达水平都非常低,甚至在部分转移性肿瘤细胞中表达消失。 通过机制研究证实了MIM蛋白通过其二聚体的形式来调控巨噬细胞对铁基材料的内吞。因此,可以通过针对MIM二聚体与细胞膜的作用机制作为靶点来设计选择性抑制巨噬细胞内吞的策略。 利用竞争性抑制的原理构建了7肽的MIM抑制剂 ,通过在材料表面修饰抑制性7肽来选择性降低MIM高表达的巨噬细胞内吞,而不降低靶部位细胞对铁基材料的摄入。

报告结束后,赵鹏博士与在座的科研工作者和研究生进行了学术交流,使大家加深了对铁基纳米材料及其应用的认识。

